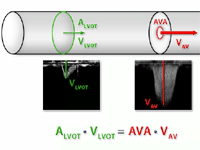
Przezcewnikowe wszczepienie zastawki aortalnej (TAVI)
Zastosowanie u chorych z ciężkim zwężeniem zastawki aortalnej i z małą objętością wyrzutową
Wśród objawowych chorych z ciężkim zwężeniem zastawki aortalnej (AS), obciążonych dużym ryzykiem operacyjnym, można wyróżnić podgrupę osób z małą objętością wyrzutową (<35 ml/m2; LFAS), z zachowaną lub obniżoną frakcją wyrzutową lewej komory (LVEF). Ważnych danych dostarczyła prospektywna analiza badania PARTNER (kohorta A – chorzy obciążeni dużym ryzykiem przydzieleni losowo do TAVI lub leczenia kardiochirurgicznego, kohorta B – chorzy zdyskwalifikowani od operacji przydzieleni losowo do TAVI lub leczenia zachowawczego).4 Wykazano, że TAVI znamiennie poprawiło przeżywalność chorych z LFAS w kohorcie B. W kohorcie A wśród pacjentów z LFAS (niezależnie od LVEF) przeżywalność po TAVI była podobna jak po leczeniu kardiochirurgicznym. Autorzy podkreślają ponadto znaczenie małej objętości wyrzutowej (≤35 ml/m2) jako niezależnego czynnika rokowniczego u chorych z ciężkim AS (w 2-letniej obserwacji całkowita śmiertelność była u nich 2-krotnie większa niż u chorych z prawidłową objętością wyrzutową).
Rokowanie krótkoterminowe
Krajowe rejestry dostarczają cennych informacji
na temat wyników TAVI. W 2013 roku opublikowano
wyniki obserwacji krótkoterminowej
(wewnątrzszpitalnej) w ramach największego europejskiego
rejestru (The German Aortic Valve
Registry – GARY).5 Prospektywnej analizie poddano
13 860 kolejnych pacjentów, u których wykonano
konwencjonalną wymianę zastawki aortalnej
(AVR, 6523 chorych), AVR z jednoczasowym pomostowaniem
aortalno-wieńcowym (AVR + CABG,
3464 chorych), TAVI z dostępu przeznaczyniowego
(TV TAVI, 2695 chorych) lub z dostępu przezkoniuszkowego
(TA TAVI, 1181 chorych). Pacjenci
kwalifikowani do TAVI byli starsi, mieli więcej
chorób współistniejących (średni wynik logistic
EuroScore 25,9% vs 8,8% dla AVR), w tym nadciśnienie
płucne i przewlekłą chorobę nerek wymagającą
leczenia nerkozastępczego. Pacjentom poddawanym
TAVI w większości przypadków wszczepiano
zastawkę CoreValve (>60% przypadków),
zabiegi dotyczyły natywnych zastawek aortalnych
(jedynie 2,1% stanowiły procedury valve-in-valve);
44% zabiegów TAVI z dostępu przeznaczyniowego
wykonywano w znieczuleniu ogólnym. Śmiertelność wewnątrzszpitalna wynosiła 2,1% dla AVR,
4,5% dla AVR + CABG, 5,1% dla TV TAVI i 7,7%
dla TA TAVI. Częstość występowania udaru niedokrwiennego
mózgu była mała we wszystkich
grupach i wynosiła odpowiednio 1,3% (AVR), 1,9%
(AVR + CABG), 1,7% (TV TAVI) i 2,3% (TA TAVI).
U 15,9% chorych poddanych TAVI stwierdzono
powikłania naczyniowe. Konieczność wszczepienia
układu stymulującego serce była najczęstsza u chorych poddanych TAVI z dostępu przeznaczyniowego
(25%) w porównaniu z dostępem przezkoniuszkowym
(11,3%), AVR (5,2%), AVR + CABG
(4,5%). U większości chorych poddanych TAVI nie
obserwowano niedomykalności aortalnej lub jedynie
niedomykalność I stopnia. Niedomykalność
drugiego stopnia stwierdzono u 7,3% w grupie TV
TAVI i u 4,0% w grupie TA TAVI.
Rokowanie długoterminowe
Od kilku lat poznajemy pochodzące z różnych ośrodków wyniki obserwacji 30-dniowych i rocznych po TAVI. W 2012 roku opublikowano analizy badania PARTNER po 2 latach od wszczepienia zastawek. W 2013 roku kanadyjscy badacze opublikowali pierwsze wyniki 5-letniej obserwacji po przezcewnikowym wszczepieniu zastawki rozprężanej za pomocą balonu.6 W ciągu 5 lat obserwowano stopniowe zwiększanie średniego gradientu przezzastawkowego (o 0,27 mm Hg/rok) oraz zmniejszenie pola powierzchni ujścia zastawki o 0,06 cm2/rok. Dysfunkcję zastawki (umiarkowaną niedomykalność lub zwężenie) stwierdzono u 3,4% osób. Udar niedokrwienny mózgu wystąpił u 9,7% pacjentów, a krwotoczny u 7,3% osób. 5-letnie przeżycie wynosiło 35%. W analizie wieloczynnikowej predyktorami zwiększonego ryzyka zgonu były obecność przewlekłej obturacyjnej choroby płuc oraz obecność co najmniej umiarkowanego przecieku okołozastawkowego po zabiegu.
Zastosowanie TAVI u chorych obciążonych umiarkowanym lub małym ryzykiem operacyjnym
Zgodnie z obowiązującymi zaleceniami zabieg TAVI należy rozważyć u objawowych pacjentów z ciasnym AS obciążonych dużym ryzykiem operacyjnym (EuroScore >20%, STS >10%).7 W praktyce klinicznej stan ogólny pacjenta oraz choroby współistniejące powodują, że decyzją zespołu ekspertów do TAVI dość często kwalifikowani są pacjenci obciążeni umiarkowanym bądź małym ryzykiem operacyjnym według obecnie używanych skal. Badacze ze Szwajcarii przedstawili wyniki TAVI w grupie takich chorych.8 Wśród 389 pacjentów poddanych zabiegowi 65,3% stanowili chorzy umiarkowanego ryzyka (STS ≥3% i ≤8%), 10,5% chorzy małego ryzyka (STS <3%), a 24,2% chorzy dużego ryzyka. Wszyscy chorzy zostali zakwalifikowani przez zespół ekspertów jako chorzy obciążeni zwiększonym ryzykiem związanym z operacją klasyczną (na podstawie obciążeń nieujętych w skali STS i Euroscore). Śmiertelność całkowita była znamiennie mniejsza u chorych małego i umiarkowanego ryzyka niż u chorych dużego ryzyka (odpowiednio 2,4% vs 3,9% vs 14,9% w obserwacji 30-dniowej i 10,1% vs 16,1% vs 34,5% w obserwacji rocznej).
W grupie małego i umiarkowanego ryzyka obserwowano również mniej istotnych zdarzeń niepożądanych w okresie okołozabiegowym (takich jak ostra niewydolność nerek) niż w grupie dużego ryzyka (odpowiednio 0% i 2,8% vs 8,5%), oraz mniej dużych powikłań związanych z miejscem dostępu naczyniowego (0% i 7,1% vs 12,8%). Nie stwierdzono natomiast znamiennych różnic pomiędzy grupami pod względem częstości powikłań krwotocznych (w obserwacji 30-dniowej) oraz udaru mózgu i zawału serca zarówno w obserwacji 30-dniowej, jak i rocznej. Opublikowano również pierwsze porównanie śmiertelności całkowitej u chorych obciążonych umiarkowanym ryzykiem poddawanych TAVI lub leczonych za pomocą operacji klasycznej.9 Analizowano dane pochodzące z 3 europejskich ośrodków (Niemcy, Szwajcaria oraz Holandia). 405 pacjentów poddanych TAVI porównano z odpowiednio dobraną grupą chorych (pod względem m.in. wieku, płci i współistniejących chorób) operowanych klasycznie. Całkowita śmiertelność zarówno 30-dniowa (7,8% dla TAVI vs 7,1% dla operacji klasycznej), jak i roczna (odpowiednio 16,5% vs 16,9%) nie różniły się istotnie statystycznie.
Problemem pozostaje konieczność wszczepienia stymulatora oraz przecieki okołozastawkowe, których częstość jest znamiennie większa w grupie TAVI. Przed rozszerzeniem wskazań do TAVI konieczne będzie również uzyskanie danych dotyczących częstości powikłań neurologicznych po TAVI i po operacji klasycznej.
Czytaj dalej: Niedomykalność zastawki mitralnej
Wady serca (postępy 2013) – spis treści
Piśmiennictwo:
(...)
4. Herrmann H.C., Pibarot P., Hueter I. i wsp.: Predictors of mortality and outcomes of therapy in low-flow severe aortic stenosis: a Placement of Aortic Transcatheter Valves (PARTNER) trial analysis. Circulation, 2013; 127: 2316–2326
5. Hamm C.W., Möllmann H., Holzhey D. i wsp.: The German Aortic Valve Registry (GARY): in-hospital outcome. Eur. Heart J., 2013 (publ. elektron. przed drukiem)
6. Toggweiler S., Humphries K.H., Lee M. i wsp.: 5-year outcome after transcatheter aortic valve implantation. J. Am. Coll. Cardiol., 2013; 61: 413–419
7. Vahanian A., Alfieri O., Andreotti F. i wsp.: Guidelines on the management of valvular heart disease (version 2012): the Joint Task Force on the management of valvular heart disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur. Heart J., 2012; 33: 2451–2496 (oprac. Med. Prakt., 2012; 12: 18–39)
8. Wenaweser P., Stortecky S., Schwander S. i wsp.: Clinical outcomes of patients with estimated low or intermediate surgical risk undergoing transcatheter aortic valve implantation. Eur. Heart J., 2013; 34: 1894–1905
9. Piazza N., Kalesan B., van Mieghem N. i wsp.: A 3-center comparison of 1-year mortality outcomes between transcatheter aortic valve implantation and surgical aortic valve replacement on the basis of propensity score matching among intermediate-risk surgical patients. JACC Cardiovasc. Interv., 2013; 6: 443–451